MICRONIZACIÓN DE MATERIALES UTILIZANDO CO2 SUPERCRÍTICO COMO AGENTE ANTIDISOLVENTE
|
Descripción |
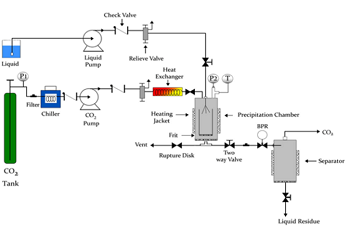
Esquema del dispositivo SAS.
Se propone una tecnología sostenible para depositar nanopartículas de metales y óxidos metálicos Se propone una tecnología sostenible para micronizar materiales libres de disolvente utilizando CO2 supercrítico como agente antidisolvente. El método se puede aplicar a la micronización de fármacos, pigmentos, polímeros, explosivos, precursores inorgánicos,… Estos compuestos son generalmente moléculas de gran tamaño o polares que tienen baja solubilidad en CO2 supercrítico mientras que se disuelven bien en disolventes orgánicos polares. La técnica se basa en el efecto antidisolvente que tiene el CO2 supercrítico al mezclarse con una disolución del compuesto a precipitar en un disolvente orgánico.
El método SAS permite controlar la morfología, tamaño y/o forma polimórfica del material precipitado variándose el disolvente y las condiciones de presión y temperatura (siempre moderadas), a la vez que produce materiales libres de disolvente.
|
¿Cómo funciona? |
Cuando el CO2 se calienta por encima de 31°C a una presión superior a 7,4 MPa se convierte en fluido supercrítico. El CO2 supercrítico tiene densidades intermedias entre las de los líquidos y los gases, pero propiedades de transporte (difusividad, viscosidad) similares a las de los gases. Cuando el CO2 entra en contacto con la disolución orgánica que contiene el soluto a micronizar y se disuelve en el disolvente, el líquido experimenta una expansión volumétrica y se convierte en un mal disolvente del soluto que precipita en forma de micro y nanopartículas. La morfología, estructura cristalina y tamaño de las partículas se controla modificando la temperatura y presión del proceso. Se obtiene partículas libres de disolvente y con una distribución estrecha de tamaños.
Un esquema del dispositivo experimental utilizado se muestra en la figura 1. Una bomba de alta presión impulsa el CO2 supercrítico a la temperatura y presión de trabajo hacia la cámara de precipitación que se halla en las mismas condiciones a flujo constante. La disolución formada por el sólido y el disolvente orgánico se introduce también a flujo constante en la cámara de precipitación a través de un nebulizador.
Las temperaturas habituales de precipitación varían entre 35 a 70 ºC, a presiones desde 8 a 20 MPa. Al disolverse el fluido en el disolvente orgánico, la mezcla que contiene el sólido se sobresatura y comienza la precipitación. La presión se controla con un regulador de presión a la salida de la cámara de precipitación. El sólido micronizado se recoge en la cámara de precipitación, mientras que la mezcla CO2 + disolvente orgánico se separa en un separador ciclónico. El precipitado se lava con CO2 supercrítico, quedando el material micronizado libre de disolvente.
Los materiales micronizados se caracterizan por rayos X (ángulo bajo y alto), análisis térmico (TGA, DTA), espectroscopia FTIR y UV-vis, microscopía electrónica (SEM y TEM), análisis de la composición por EDX y microanálisis,… También se realizan ensayos de velocidad de disolución de los fármacos.
Con esta técnica ya hemos micronizado fármacos como el diflunisal (DF- analgésico antinflamatorio), así como formulaciones farmacéuticas como la formada por DF y el polímero PVP, y el co-cristal formado por el DF con nicotinamida (NIC- compuesto soluble en agua de la familia de vitamina B). La figura 2 muestra imágenes SEM de los materiales, En todos los casos las formulaciones preparadas mostraron mejoras en la velocidad de disolución frente a los fármacos puros debido al cambio de propiedades de la formulación y al control de la morfología y tamaño obtenidos por el proceso SAS.
|
Ventajas |

Fármacos precipitados por SAS.
Las técnicas tradicionales de micronización como la trituración, cristalización, “spray-drying” o “freeze drying” presentan varias limitaciones como el escaso control del tamaño de las partículas y la temperatura elevada que se puede necesitar para eliminar el disolvente. Por el contrario, la precipitación por el método SAS produce materiales libres de disolvente a la vez que se puede controlar la morfología, tamaño y/o forma polimórfica del material precipitado.
El CO2 es considerado como un disolvente sostenible al tener parámetros críticos moderados, ser barato, inocuo, incombustible y poder ser reciclado. Además, el CO2 es un gas en condiciones atmosféricas que se elimina fácilmente del material por simple despresurización y no deja residuos.
|
¿Dónde se ha desarrollado? |
La técnica se ha desarrollado en el Laboratorio de Equilibrio de Fases y Fluidos Supercríticos de la Facultad de Ciencias Químicas en la Univesidad Complutense de Madrid (UCM) por el grupo de investigación “Preparación y Actividad de materiales multifuncionales y procesos Físicoquímicos en Química Sostenible” que trabaja en la preparación de materiales utilizando fluidos supercríticos como alternativa a los disolventes comunes más contaminantes. Además de tratarse de procesos más sostenibles, los materiales que se obtienen presentan mejores propiedades que los obtenidos por métodos convencionales. El grupo tiene amplia experiencia en el área de fluidos supercríticos, tanto desde un punto de vista fundamental como aplicado.
|
Y además |
El grupo pertenece a la Real Sociedad Española de Química (RSEQ), la asociación española de fluidos comprimidos (FLUCOMP), la “International Society for the Advancement of Supercritical Fluids” (ISSASF) y la Red Española de Química Sostenible.
Se ofrece iniciar colaboraciones con empresas y/u otros grupos de investigación con el objetivo de utilizar esta técnica en aquellos casos en los que las técnicas convencionales no produzcan resultados satisfactorios, con el fin de obtener productos de alto valor añadido. El grupo dispone de un precipitador SAS por efecto antidisolvente para llevar a cabo experimentos de micronización a escala de laboratorio, así como de equipos de caracterización de los materiales producidos. Ofrecemos otras ofertas de transferencia tecnológica basadas en el uso de CO2 supercrítico.
|
Contacto |
|
© Oficina de Transferencia de Resultados de Investigación – UCM |
|
Descargas PDF |
|
Clasificación |
|
Investigadoras responsables |
Albertina Cabañas Poveda: a.cabanas@quim.ucm.es
Concepción Pando García-Pumarino: pando@quim.ucm.es
Departamento: Química-Física I
Facultad: Ciencias Químicas